(دکتر مریم اسلامی)
در این شماره از مجله، راهنما و همکاران 1 نتایج یک کارآزمایی بالینی فاز 3 برماژن ژپرپاوک VEc-B را به عنوان ژن درمانی موضعی گزارش می کنند. در برگه جدیدی برای اپیدرمولیز بولوزا دیستروفیک، یک بیماری تاول ژنتیکی نادر اما تهدید کننده زندگی باز می شود. در یک سرمقاله همراه، Schaffer2 پیامدهای این یافته ها را برای تحقیقات آینده مورد بحث قرار می دهد.
اپیدرمولیز بولوزا دیستروفیک چیست؟
دیستروفیک اپیدرمولیز بولوزا، یک بیماری نادر که تقریبا 1 تا 3 نفر در هر میلیون را در ایالات متحده تحت تاثیر قرار می دهد، 3 ناشی از جهش در COL7A1 است که زنجیره آلفا-1 کالژن نوع VII را کد می کند. در پروتئین زبانه جدید ( (C7باز می شود (به مفاهیم کلیدی مراجعه کنید) که فیبریل های لنگر پوست و غشاهای مخاطی را تشکیل می دهد. (شکل 1)
پوستشان که با کوچکترین تماسی پاره می شود. ضربه های جزئی ناشی از فعالیت های روزمره به طور مکرر باعث ایجاد تاول و زخم در بافت های اپیتلیال می شود که منجر به تنگی های مری و ادراری تناسلی، بدشکلی انگشتی ناشی از چسبندگی انگشتان دست، سوء تغذیه، کم خونی و عفونت می شود. خارش و درد می تواند ثابت باشد و کیفیت زندگی را کاهش دهد. علاوه بر این، زخمهای مزمن میتوانند سرطان های سلول سنگفرشی تهاجمی را ایجاد کنند که عامل اصلی مرگ در بزرگسالان مبتلا به اپیدرمولیز بولوزا دیستروفیک است.
چگونه جهش های COL7A1 باعث ایجاد تاول می شوند؟
C7 یک پروتئین میلهای شکل دراز است که به دور خود میپیچد و یک مارپیچ سه گانه را تشکیل می دهد، که به طور کووالانسی به یک مارپیچ سه گانه دیگر C7 در جهت مخالف می پیوندد و سپس انباشته می شود و فیبرهای لنگر را تشکیل می دهد. این فیبریل ها در یک الگوی U شکل در ناحیه غشای پایه اپیتلیال قرار می گیرند، جایی که با پروتئین های اطراف تعامل می کنند تا اپیتلیوم را به بافت همبند زیرین متصل کنند.
A.1 شکل
جهش های COL7A1 میتوانند در یک الگوی مغلوب یا غالب به ارث برده شوند یا ممکن است به طور ناگهانی ایجاد شوند. شکل مغلوب اپیدرمولیز بولوزا دیستروفیک به دلیل از دست دادن عملکرد یا جهش های پوچ در نسخه های ارثی COL7A1 از مادر و پدر ایجاد می شود که منجر به نقص، کاهش یا عدم وجود C7 می شود. در شکل غالب، جهش ها در یک کپی از ژن، پروتئین های فاسد C7 را ایجاد می کنند که مونتاژ طبیعی C7 را مختل می کنند و در تشکیل فیبریل لنگر دخالت می کنند. شدت بیماری بر اساس میزان درگیری پوستی و خارج پوستی تعیین می شود و با تأثیر جهش ها بر تعداد و عملکرد فیبرهای لنگر مرتبط است.
B-VEC چیست؟
B-VEC یک ژن درمانی موضعی است که از دو نسخه از توالی کد کننده COL7A1 تشکیل شده است که درون یک ویروس هرپس سیمپلکس اصلاح شده نوع 1 ( 1-HSV) کپسوله شده است. در وکتور تب جدید باز می شود. 1-HSV عامل سرماخوردگی است، اما تغییرات ناقل پاسخ های التهابی میزبان را محدود می کند و از تکثیر ویروس جلوگیری می کند، در نتیجه توانایی آن را برای ایجاد بیماری مسدود می کند. برای دستیابی به تحویل ژن، پروتئین های روی پوسته بیرونی ناقل -HSV1 با پروتئینهای بیان شده در سطح سلولهای پوست تعامل می کنند تا ورود نوکلئوکپسید ویروسی را تسهیل کنند. هنگامی که داخل سلول قرار می گیرد، DNA ویروسی رونویسی و به C7 ترجمه می شود، که به فضای خارج سلولی ترشح می شود تا به فیبریل های لنگر متصل شود (شکل 1). Bژنوم ویروسی 1-HSV به طور دائم در DNA میزبان ادغام نمی شود – با هر تقسیم سلولی رقیق می شود. بنابراین، اثرات درمانی -B VEC گذرا است و برای کنترل طولانی مدت بیماری، تجویز مکرر مورد نیاز است. اگرچه ژن درمانی تحت هدایت پوست به تظاهرات خارج جلدی
اپیدرمولیز بولوزا دیستروفیک نمی پردازد، VEC-B دارای چندین مزیت به عنوان ژن درمانی برای این بیماری است. اول، وکتورهای مبتنی بر 1-HSV میتوانند درجهای ژنی بزرگی مانند COL7A1 را در خود جای دهند، که با اندازه 9 کیلوبایت از ظرفیت اکثر ناقلهای دیگر مورد استفاده برای ژن درمانی فراتر میرود. دوم، چون VEC-B اپیزومی (یعنی خارج کروموزومی) در داخل سلول میزبان باقی می ماند، از خطر جهش زایی درج جلوگیری می شود. سوم، VEC-B در یک ژل متیلسلولز فرموله شده است که به بیماران اجازه می دهد تا دارو را به صورت موضعی برای بهبود زخم در محیط سرپایی استفاده کنند. این ویژگی باعث میشود VEC-B راحتتر از سلول درمانی های مهندسی شده با COL7A1 که شامل بیهوشی، روشهای جراحی یا بستری شدن در بیمارستان برای درمان است.
B-VEC چقدر خوب کار می کند؟
کارآزمایی انجام شده توسط گاید و همکاران. یک کارآزمایی فاز 3، دوسوکور، درون بیمار، تصادفی شده و کنترل شده با دارونما از VEC-B شامل 31 بیمار مبتلا به اپیدرمولیز بولوزا دیستروفیک (30 با فرم مغلوب و 1 با فرم غالب) بود. (تقریبا 70 درصد از زخمهایی که در معرض VEC-B قرار گرفتند، در 6 ماهگی بسته شدند) از جمله در بیمار مبتلا به اپیدرمولیز بولوزا دیستروفیک غالب(، در مقایسه با تقریبا 20 درصد زخمهایی که در معرض دارونما قرار گرفتند. علاوه بر این، دوام
بهبود زخم (تعریف شده به عنوان بسته شدن کامل زخم در هر دو ماه 3 و 6 )در 50 ٪از زخم های در معرض VEC-B ،در مقایسه با 7 ٪از زخم های در معرض دارونما مشاهده شد. در یک مطالعه قبلی فاز 1-2 ،میکروسکوپ الکترونی نمونه های بیوپسی پوست به دست آمده از بیماران مبتلا به اپیدرمولیز بولوزا دیستروفیک مغلوب نشان داد که VEC-B بیان
C7 را در رنگآمیزی ایمونوفلورسانس در ناحیه غشای پایه و تشکیل فیبریل های لنگر القا میکند. ژن درمانی موضعی با VEC-B ناهنجاری های هیستوپاتولوژیک و فراساختاری در پوست بیماران مبتلا به اپیدرمولیز بولوزا دیستروفیک را معکوس می کند (شکل 1(.C
خطرات چیست؟
از نظر تئوری، واکنش های التهابی به VEC-B یا ژل وسیله نقلیه آن ممکن است رخ دهد، اگرچه تغییرات ناقل برای کاهش خطر التهاب طراحی شده است. در کارآزمایی توسط گاید و همکاران، 7 درصد از بیماران پس از تجویز VEC-B دچار اریتم یا بثورات پوستی شدند. با این حال، هیچ یک از کارآزمایی انصراف ندادند، و هیچ اثر سمی سیستمیک یا عوارض جانبی جدی مربوط به VEC-B گزارش نشد.
ایمنی زایی در برابر 1-HSV و C7 می تواند منجر به رد ایمنی سلول های ناقل یا انتقال یافته توسط ناقل شود و در نتیجه با درمان های مکرر کارایی کاهش یابد. علاوه بر این، آنتی بادی ها علیه C7 ممکن است نشان دهنده ایجاد یک اختلال تاول زای خود ایمنی ثانویه به نام اپیدرمولیز باشند که معمولا درمان طولانی مدت سرکوب کننده ایمنی بولوزا اکویزیتا درمان طولانی را تضمین می کند. افزایش در تیتر آنتی بادیها علیه 1-HSV و C7 تقریبا در تمام بیمارانی که در ابتدا سرم مثبت بودند مشاهده شد و آنتی بادی ها علیه (1-HSV یا C7یا هر دو ) در حدود 75 درصد از بیماران سرم منفی تا هفته 26 ایجاد شد. از درمان VEC-B ،اگرچه هیچ ارتباطی بین ایمنی زایی و شکست درمان شناسایی نشد.
بعدی چیه؟
فراتر از VEC-B ،چندین رویکرد با هدف بازگرداندن عملکرد C7 وارد توسعه بالینی برای درمان اپیدرمولیز بولوزا دیستروفیک شده است. کارآزماییهای فاز 1-2 در حال حاضر در حال ارزیابی کراتینوسیتهای اتولوگ مهندسی شده با COL7A1 هستند 6 ( شماره gov.ClinicalTrials. ،NCT04227106در برگه جدید باز می شود) یا فیبروبالستها 7. ( NCT04213261باز می شود. در برگه جدید باز می شود( و درمان داخل وریدی در محل باز NCT502 پروتئین .2-C75
.(همه رویکردها اثرات بیولوژیکی و درمانی اولیه را نشان داده اند) تعریف شده به عنوان بسته شدن زخم ≤50٪) با برخی از زخم های پیوند کراتینوسیت اصلاح شده با COL7A1 که 75 درصد یا بیشتر بهبود زخم را نشان میدهند که تا 5 سال طول می کشد. 6 تداوم طولانی مدت اصلاح ژن سلولها و پیامدهای ایمنی زایی نیاز به ارزیابی بیشتر در گروه بزرگتری از بیماران دارد. نشان داده شده است که کاربرد موضعی یا داخل جلدی جنتامایسین باعث بیان C7 تمام قد، تشکیل فیبریل های لنگر، و بهبود زخم در بیماران مبتلا به اپیدرمولیز بولوزا دیستروفیک مغلوب از طریق پرش اگزون می شود، مکانیزمی که اثر یک جهش بیماری زا را سرکوب می کند. با القای برش آن (یا بهتر است بگوییم، بخشی که در آن قرار دارد) از RNA پیام رسان. این یافته منطق ارزیابی بالینی الیگونوکلئوتیدهای آنتی سنس موضعی را تقویت می کند که رد اگزون را برای درمان اپیدرمولیز بولوزا دیستروفیک القا می کنند، که در یک کارآزمایی در حال ارزیابی است (.NCT05529134در برگه جدید باز می شود).
آیا موفقیت بالینی VEC-B به عنوان درمان اپیدرمولیز بولوزا دیستروفیک می تواند به سایر بیماری های ژنتیکی ترجمه شود؟ ملاحظات شامل ناتوانی ناقل 1-HSV در نفوذ به پوست دست نخورده، توانایی ژن درمانی های موضعی برای هدف قرار دادن سلول های مناسب برای بازگرداندن بیان عملکردی (متعادل در برابر خطر بیان پروتئین نابجا به دلیل انتقال سلول های هدف ناخواسته)، و اهمیت نسبی نجات عملکرد ژن در اپیتلیوم هدف در بیماری های ژنتیکی با تظاهرات سیستمیک با در نظر گرفتن این عوامل، ژنودرماتوزهای با مانع پوستی مختل، مانند مواردی که در
ایکتیوزهای مادرزادی، درماتیت آتوپیک و اپیدرمولیز بولوزای جانکشنال به دلیل نقص در لامینین ترشحی دیده می شود، به خط مقدم می رسند. فرموالسیون برای زایمان چشمی، دهانی- گوارشی یا تنفسی برای پرداختن به تظاهرات خارج جلدی اپیدرمولیز بولوزا و سایر بیماری های ژنتیکی ارزش زیادی دارد، اگرچه تحویل ژن درمانی موضعی به اپیتلیوم ریه از نظر تاریخی به دلیل پاکسازی مخاطی، التهاب، چالش برانگیز بوده است. و عدم نفوذ به دلیل اتصالات محکم بین
سلول های اپیتلیال راه هوایی. اخیرا ، حامی VEC-B از ترخیص یک برنامه دارویی جدید تحقیقاتی برای یک ژن درمانی موضعی برای فیبروز کیستیک خبر داد که توسط یک نبوالیزر در یک کارآزمایی در حال انجام ارائه می شود. (.NCT05504837در برگه جدید باز می شود.) در نهایت، تکمیل کارآزماییهای بالینی مانند این مورد برای تعیین اینکه
آیا انتقال ژن با واسطه 1-HSV میتواند بیشتر از عمق پوست باشد، مورد نیاز است.
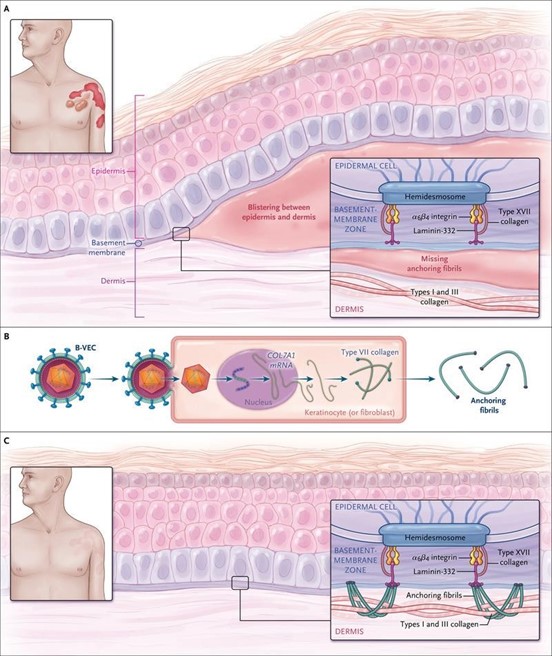
شکل 1 .نقش ژن درمانی (VEC-B (Geperpavec Beremagene در اپیدرمولیز بولوزا دیستروفیک

