(دکتر مریم اسلامی)
استفاده از آهن برای کمک به از بین بردن سلول های مقاوم در (سرطان پروستات مقاوم به درمان)
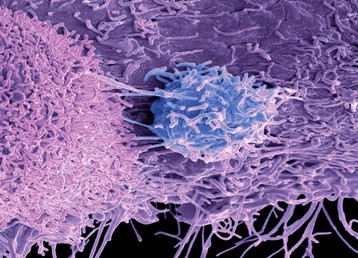
میکروگراف الکترونی اسکن رنگی از سطح سلول های سرطانی پروستات. سلول ها فرآیندهای متعدد و میکروویلی ها (برجستگی های سطحی ریز) را نشان می دهند. این ویژگی ها مشخصه سلولهای بسیار متحرک هستند و سلول های سرطانی را قادر میسازند تا به سرعت در بدن متاستاز کنند. بزرگنمایی: 8000 x هنگام چاپ در عرض 01 سانتی متر.
یک تیم تحقیقاتی بر این باورند که یکی از راههای از بین بردن سلول های مقاوم در برابر سرطان پروستات،
استفاده از آهن زیاد است. چونه ونگ یان، دکترای زیست شناس مولکولی در مرکز سرطان جورجیا،
می گوید: فلزی که کلید گلبول های قرمز خون است که اکسیژن و سایر مواد اولیه بدن را حمل می کنند، همچنین برای سلول ها در مقادیر زیاد کشنده است، اما سلول های سرطان پروستات اساساً در برابر آن غیرقابل نفوذ هستند. (بخش بیوشیمی و بیولوژی مولکولی در کالج پزشکی جورجیا (MCG)). یان در حال تنظیم یک استراتژی برای تغییر آن و امکان مرگ با آهن برای سرطان پروستات مقاوم به درمان از طریق فرآیند مرگ سلولی به نام فروپتوزیس است. علیرغم ضروری بودن، مقادیر زیادی آهن همچنین سطوح بالایی از (رادیکال های آزاد سمی (ROS)) تولید می کند که پیامدهای آن شامل آسیب رساندن به لیپیدها یا چربیها است که برای عملکرد سلول ضروری هستند.
یان، محقق اصلی جایزه 1.1 میلیون دالری توسعه ایده جدید از سوی وزارت دفاع ایاالت متحده، می گوید:
«زمانی که سلول آهن را جذب می کند، فرآیندهای مختلفی را طی می کند که ROS زیادی تولید می کند.
در حالی که تعامل آهن و ROS معمول است، وقتی سطح هر دو بالا باشد، به لیپیدها، جزء مهم غشای سلولی، آسیب می رساند. یان می افزاید: « کاری که ما در تالش هستیم انجام دهیم این است که از این عارضه جانبی برای درمان سرطان پروستات استفاده کنیم.
از طریق این فرآیند پراکسیداسیون لیپیدها، لیپیدها که همچنین ذخیره انرژی مهمی برای سلول ها و سیگنال دهی داخلی سلولی هستند، تجمع مییابند، انعطاف پذیری و کارایی خود را از دست می دهند و در نهایت سلول می میرد، اگرچه دقیقاً دلیل آن یک راز باقی مانده است.
این تغییرات چربی مخرب هستند، اما سرطان پروستات می تواند به ویژه نسبت به آنها و داروهایی که برای ایجاد این نوع آسیب آهن اضافی طراحی شده اند، حساس نباشد، زیرا سلول های سرطانی در حال حاضر به تغییرات مشابهی در لیپیدهای غشای سلولی نیاز دارند تا اطمینان حاصل شود که مقدار زیادی از آنها را دارند. انرژی مورد نیاز آنها برای زنده ماندن، رشد و گسترش است.

چونهونگ یان، دکترا، مرکز سرطان جورجیا و کالج پزشکی جورجیا [مایکل هوالهان/دانشگاه آگوستا]
اما تیم تحقیقاتی MCG دریافته است که ژن ATF3، تنظیم کننده استرس سلولی که آنها همچنین نشان داده اند می تواند سرطان پروستات را سرکوب کند، می تواند سلول های سرطانی پروستات را نسبت به ترکیب جدیدتر JKE-1674 آسیب پذیرتر کند که می تواند به القای فروپتوز کمک کند.
یان خاطرنشان می کند که اساسًا، اگر توانایی سلول های سرطانی پروستات در نادیده گرفتن استرس را کاهش دهید، می میرند.
قطعه دیگری از پازلی که آنها پیدا کرده اند این است که داروی بورتزومیب، یک عامل شیمی درمانی که برای درمان مولتیپل میلوما استفاده می شود، شریک خوبی است زیرا می تواند بیان ATF3 یا فعال کننده فاکتور رونویسی 3 را افزایش دهد. ATF3 به نوبه خود باعث بیان HMOX1 می شود. آنزیم و آنتی اکسیدان شناخته شده ای که اساسا آهن را از جاهایی مانند هموگلوبین جدا می کند تا بیشتر در داخل سلول ها تجمع پیدا کند که کشنده است.
یک قطعه دیگر مکانیسم طبیعی بدن برای مقابله با این جفت ناسالم آهن و ROS است به طوری که بسیاری از سلول های خوب در نتیجه نمی میرند. به آن گلوتاتیون پراکسیداز 4 یا GPX4 می گویند که یک آنتی اکسیدان و مهارکننده فروپتوز است. یکی از راه های کار JKE-1674 مهار GPX4 است که مزیت اضافه ترمیم بخشی از آسیب به لیپیدها را دارد که سلول های سرطانی پروستات را نسبت به مرگ در اثر فروپتوز حساس نمی کند. به گفته یان، این نوع از مهارکننده ها قبالً در درمان سرطان نویدبخش بوده اند.
یان خاطرنشان می کند که آزمایشات بالینی نشان داد که بورتزومیب به ویژه در درمان سرطان پروستات مؤثر نیست، اما در ترکیب با JKE-1674، آنها شواهد آزمایشگاهی دارند که به دشمنی قدرتمند در برابر سرطان رایج تبدیل می شود.
در یک کشت سلولی، تیم یان افزایش بیان ATF3 را مشاهده کرده است که سلول های سرطانی پروستات انسانی را با آهن حساس می کند، و مطالعات جدید با بودجه وزارت دفاع آمریکا مراحل بعدی را ممکن می سازد: مطالعه القای موش مبتلا به سرطان پروستات انسانی، به نام مدل موش انسانی. برای مشاهده اینکه آیا بورتزومیب ناشی از ATF3 همراه با JKE-1674 دوباره باعث ایجاد فروپتوز در سرطان پروستات پیشرفته و معمولا کشنده می شود یا خیر.
آنها همچنین یک موش دستکاری شده ژنتیکی جدید دارند که ATF3 بیشتری تولید می کند و خواهند دید که
آیا سرطان پروستات را نیز در برابر فروپتوز آسیب پذیرتر می کند یا خیر.
یان و همکارانش همچنین میخواهند در مورد اینکه چگونه ATF3 سلولهای سرطانی پروستات را با کمک عواملی مانند بورتزومیب در برابر مرگ توسط آهن آسیب پذیرتر می کند، بیاموزند.
آزمایشگاه یان از داروها و رژیم های دارویی موجود برای شناسایی مؤثر درمانی استفاده میکند که میتواند نسبتاً سریع از آزمایشگاه او به کارآزمایی بالینی برای سرطان شایعترین سرطان در مردان آمریکایی، به غیر از سرطان پوست غیر مالنوما، و دومین عامل اصلی سرطان تبدیل شود. به گفته انجمن سرطان آمریکا، مرگ، پشت سرطان ریه.
برای اطلاعات بیشتر در مورد فروپتوز به عنوان یک شکل متمایز از مرگ سلولی، به GEN مراجعه کنید: “کلسترول بالا سوخت متاستاز سرطان با تقویت مقاومت در برابر شکلی از مرگ سلولی و مکانیسمی که توسط کدام اسید چرب امگا 3 “سم” برای تومورها است. همچنین به «سلول های سرطانی که در اثر فروپتوز میمیرند، ایمنی ضد تومور با واسطه سلول های دندریتیک را مختل می کنند.»
«هدفهای دارویی برای القای فروپتوز: تمرکز بر نوروبالستوما و گلیوبالستوما» (مرزها در انکولوژی) را ببینید.
https://www.genengnews.com/topics/cancer/using-iron-to-help-kill-resistant-/prostate-cancer-cells